https://www.tohoku.ac.jp/japanese/2024/07/press20240702-01-dna.html
2024年 | プレスリリース・研究成果
【本学研究者情報】
〇多元物質科学研究所 助教 岡村秀紀/教授 永次史
研究室ウェブサイト
【発表のポイント】
- 化合物に応答して二重鎖DNAの形成と解離を自在に制御できる新規人工核酸を開発しました。
- この人工核酸を用いて、in vitro(注1)で遺伝子発現を可逆的に制御することに成功しました。
- 遺伝子発現を基盤とする合成生物学研究やバイオテクノロジーの開発に貢献できるほか、高精度な遺伝子治療への応用が期待されます。
【概要】
DNAに保存された遺伝情報をもとにRNA(注2)を経てタンパク質が生成される過程は遺伝子発現と呼ばれ、最も基本的な生命現象です。近年、遺伝子を人工的に設計・合成することが可能となり、人工遺伝子を用いた基礎研究やバイオテクノロジーの開発が大きな潮流を生み出しています。これら人工遺伝子を用いる研究においては、その発現を精密に制御する技術が必要不可欠です。しかし、これまでに報告されている制御法は、効率や生体適用性が不十分であり、新たな手法の開発が必要と考えられていました。
東北大学多元物質科学研究所(東北大学大学院理学研究科化学専攻 兼担)の岡村秀紀 助教、永次史 教授、大学院生の矢尾健行 氏(大学院理学研究科化学専攻)は、特定の化合物の添加に応答して、遺伝子発現を可逆的に制御可能な人工核酸の開発に成功しました。これらの人工核酸は、ホスト--ゲスト相互作用(注3)による可逆的な結合を通じて二重鎖の解離と形成を制御することにより、転写過程のOFF--ONを精密に切り替えます。本研究で用いたホスト-ゲスト相互作用は、生体条件下でも機能します。そのため、本人工核酸を用いることで、生体深部における遺伝子発現制御を実現できる可能性があり、遺伝子発現を基盤とするバイオテクノロジーや治療法の高精度化につながることが期待されます。本研究成果は、科学誌Journal of the American Chemical Societyのオンライン版に2024年6月28日に掲載されました。
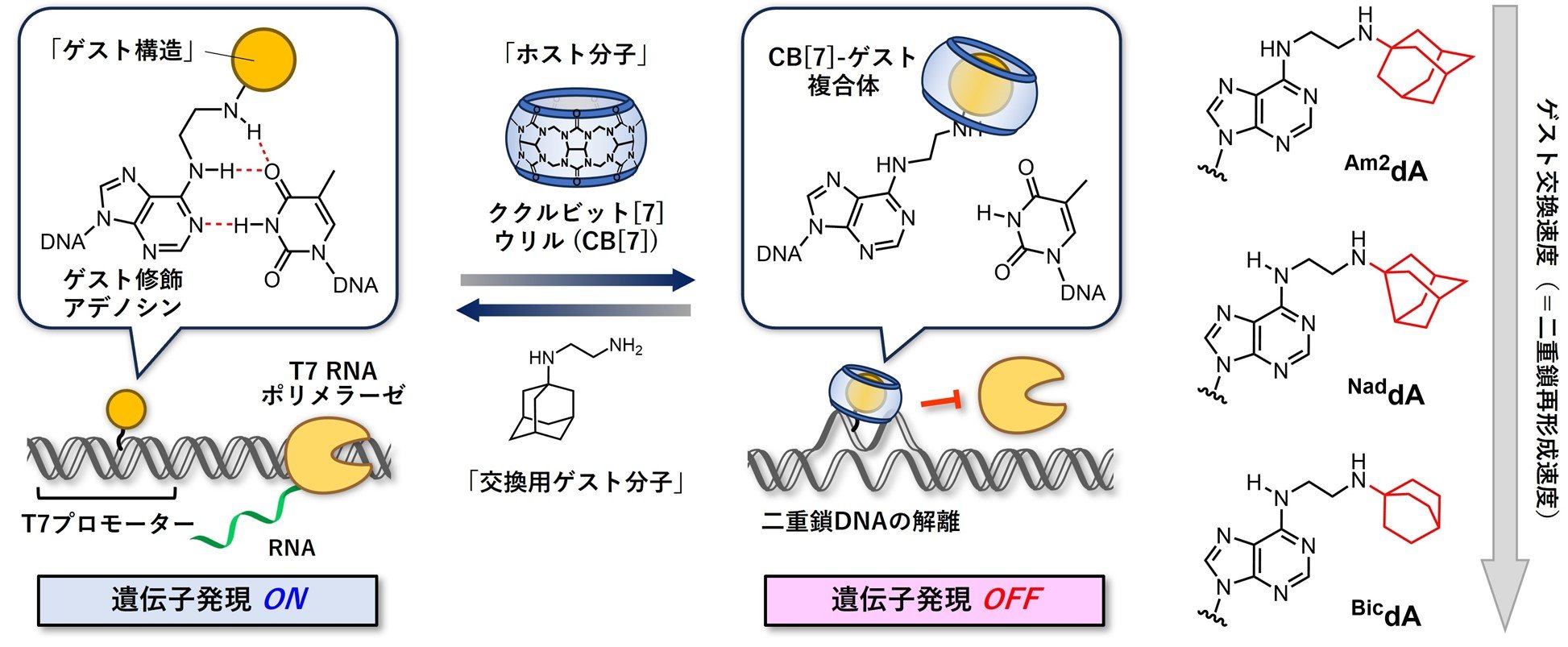
図1. ホスト-ゲスト相互作用によって二重鎖DNAを解離・再形成できるゲスト修飾アデノシンの設計と遺伝子発現の可逆制御への応用。
【用語解説】
注1. in vitro:「試験管内で」という意味。生化学実験等において、試験管内で生体内に準ずる環境を人工的に作り、実験を行うことを示す。
注2. RNA:リボ核酸の略。タンパク質をコードするメッセンジャーRNAのほか、コードしないノンコーディングRNAも存在し、その種類ごとに様々な機能を持つ。
注3. ホスト--ゲスト相互作用:ホスト(受容体)分子とゲスト(リガンド)分子の間で起こる特異的な相互作用のこと。ホスト分子とゲスト分子は、静電相互作用やファンデルワールス相互作用といった非共有結合によって結合するため、可逆的な結合性を示す。
問い合わせ先
東北大学多元物質科学研究所
助教 岡村 秀紀(おかむら ひでのり)
(理学研究科化学専攻 兼担)
電話:022-217-5634
Email:hidenori.okamura.b8*tohoku.ac.jp(*を@に置き換えてください)
東北大学多元物質科学研究所
教授 永次 史(ながつぎ ふみ)
(理学研究科化学専攻 兼担)
電話:022-217-5633
Email:fumi.nagatsugi.b8*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学多元物質科学研究所 広報情報室
電話:022-217-5198
Email:press.tagen*grp.tohoku.ac.jp(*を@に置き換えてください)

![]()
東北大学は持続可能な開発目標(SDGs)を支援しています

0 件のコメント:
コメントを投稿